경제
셀트리온, 휴마시스 코로나19 신속진단키트 미 FDA 긴급사용승인
박서진 기자
승인 2021.04.19 15:47
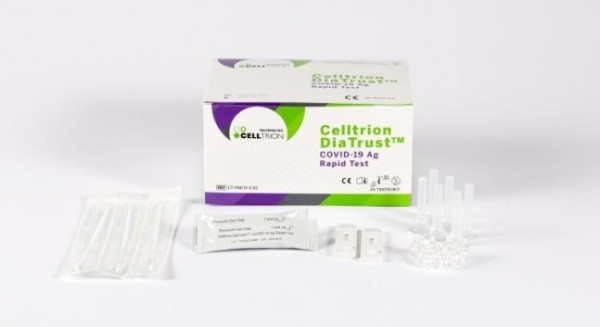
[사진 = 셀트리온 제공]
셀트리온은 체외진단 전문기업 휴마시스와 공동개발한 코로나19 현장형항원신속진단키트 '디아트러스트'(Celltrion DiaTrust COVID-19 Ag Rapid Test)가 미국 식품의약국(FDA)의 긴급사용승인을 획득했다고 19일 밝혔다.
디아트러스트는 코로나19 바이러스 항원을 인식해 감염 여부를 15분 이내에 진단하는 전문가용 제품이며, 미국에서 코로나19 초기 감염자를 대상으로 확인한 결과, 양성 환자를 양성으로 인지하는 민감도는 93.3%로 확인됐다.
이번 승인을 통해 연속검사(Serial Testing)도 함께 허용됐다. 3일에 한 번씩 혹은 24시간에서 36시간 간격을 두고 일주일에 2회 코로나 검사를 진행할 수 있게 됐다.
셀트리온은 향후 자가진단키트의 수요가 늘어날 수 있다는 판단에 따라 미국에서 450여 명을 대상으로 임상시험을 하고 그 결과를 FDA에 제출했다.
[저작권자 (c)찾아가는 뉴미디어 서치인, 무단전재 및 재배포 금지]